根据国际权威医学期刊JAMA发表了关于2013-2018年中国糖尿病患病和治疗状况的研究,结果显示,中国成人糖尿病患病率和前期患病率在短短五年竟上涨约4个百分点!据统计,2013年-2018年我国糖尿病患病率从10.9%增加到12.4%,与此同时,女性的糖尿病患病率均低于男性。糖尿病患病率也随着年龄的增长而增加:18-29岁人群患病率在五年间仍维持为5.0%,70岁以上人群患病率从2013年的20.7%上调至2018年的27.3%。值得注意的是,糖尿病前期患病率也在增高,并于2018年达到38.1%,这提示更多的人群存在潜在风险。总而言之,糖尿病和糖尿病前期总患病率已经达到50.5%!
T2DM 是由损害 β 细胞功能和胰岛素作用的遗传因素和环境因素之间的相互作用引起的。糖尿病在临床上是通过血浆葡萄糖水平升高来诊断的,然而,β 细胞功能的丧失会随着时间的推移而逐渐丧失,并且到临床诊断糖尿病时,β 细胞功能障碍已经严重了。糖耐量受损患者的正常 β 细胞功能 <50% ,而 T2DM 患者的胰岛素抵抗程度则低于正常 β 细胞功能的 15%,这表明 β 细胞功能的渐进性-T2DM 过程中的细胞功能障碍。因此,保留或恢复 β 细胞功能的方法对于我们预防和治疗 T2DM 的尝试非常重要。
2 型糖尿病的发病机制
1、β细胞对胰岛素抵抗的补偿
血浆葡萄糖水平由组织对胰岛素的敏感性以及胰腺β细胞分泌的胰岛素量决定。许多因素,包括缺乏运动、肥胖和内脏脂肪,是胰岛素抵抗的主要决定因素。通常,胰岛素抵抗的增加与β细胞胰岛素分泌的代偿性增加相匹配,胰岛素抵抗和胰岛素分泌之间的关系由双曲线定义。
基于这种双曲线关系,β细胞补偿可以通过处置指数来确定,处置指数定义为胰岛素分泌和胰岛素敏感性的乘积。只要胰岛素分泌乘以胰岛素敏感性的乘积保持恒定,葡萄糖耐量就得以保留。例如,对于一个瘦的、胰岛素敏感的个体来说,维持正常的血糖水平需要较少的胰岛素分泌。肥胖、胰岛素抵抗的个体需要代偿性增加胰岛素分泌,以维持正常的血糖水平。β 细胞对胰岛素抵抗的补偿不足会导致葡萄糖稳态受损,并最终导致 T2DM。
2、糖毒性和脂毒性
糖毒性是指由长期升高的葡萄糖水平引起的对胰腺β细胞的不可逆损伤,并已在体外和体内研究中得到证实。
与长期升高的葡萄糖水平类似,长期升高的游离脂肪酸(FFA)水平已知会导致β细胞功能障碍,这一概念称为脂毒性。
肥胖,尤其是腹部肥胖,过度膨胀的脂肪组织,会导致 FFA 水平升高,并已被证明与胰岛素基因表达降低和 β 细胞死亡相关。使用脂质输注的体外和体内研究表明,长期接触 FFA 会导致葡萄糖刺激的胰岛素分泌减少、胰岛素基因表达减少以及 β 细胞系和分离的人胰岛中的 β 细胞凋亡增加。
最近,“糖脂毒性”的概念被引入,因为有证据表明脂毒性取决于同时存在的高血糖,并且升高的葡萄糖和 FFA 协同作用损害 β细胞功能。
3、内质网压力
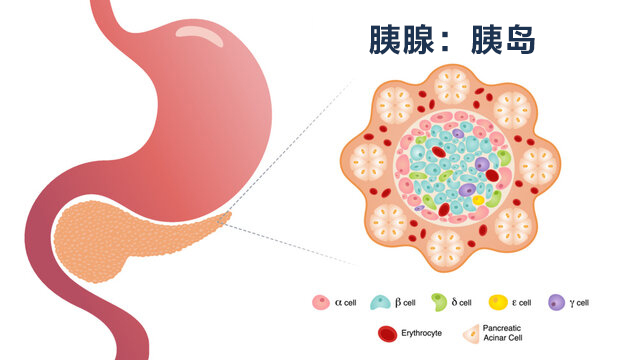
内质网(ER) 是负责蛋白质折叠(从无规则卷曲折叠成特定的功能性三维结构)、修饰和运输的细胞器。β细胞具有分泌功能,其内质网特别丰富。当内质网的折叠能力无法与蛋白质负载相匹配时,就会发生内质网应激,并且未折叠或错误折叠的蛋白质会在内质网管腔中积聚。慢性高血糖会增加β细胞的生产需求,从而使它们面临内质网应激的风险。由于高血糖个体的 β 细胞会增加前胰岛素原的产生以应对血糖水平升高,错误折叠的胰岛素原可能会导致 ER 应激。
当内质网应激发生时,许多不同的应激反应统称为未折叠蛋白反应(UPR)被激活,试图恢复细胞功能。这是通过以下方式实现的:(a) 翻译减少,(b) 内质网折叠能力增加,(c) 内质网应激相关的蛋白质降解,以及最终 (d) 。如果 a、b 和 c 不成功的话细胞凋亡。
4、氧化应激
体外和体内研究表明氧化应激与葡萄糖诱导的 β 细胞功能障碍有关。当葡萄糖通过氧化磷酸化在线粒体中代谢时,会产生活性氧(ROS)。正如涉及大鼠胰岛的研究表明,ROS 降低线粒体产生 ATP 的能力,从而减少葡萄糖刺激的胰岛素分泌。与来自非 T2DM 对照的胰岛相比,来自 T2DM 患者的孤立胰岛的氧化应激标志物有所增加,并且氧化应激水平与葡萄糖刺激的胰岛素分泌受损程度相关。此外,暴露于抗氧化剂谷胱甘肽24小时可显着改善葡萄糖刺激的胰岛素释放,并导致氧化应激标志物减少,这表明减少胰岛细胞氧化应激可能会改善T2DM胰岛的功能损伤。
5、 β 细胞质量减少
许多研究表明,T2DM 患者的 β 细胞质量和/或体积减少 。在一项对 124 例尸检胰腺组织进行检查的研究中,发现与没有2型糖尿病的瘦人相比,肥胖个体的相对 β 细胞体积增加了 50%。相比之下,与非2型糖尿病的肥胖个体相比,空腹血糖受损 (IFG) 的肥胖者的 β 细胞体积减少 40%,而患有2型糖尿病的肥胖者的 β 细胞体积减少 63% 。相应的非糖尿病对照组相比,瘦的 2 型糖尿病患者的 β 细胞凋亡频率增加了 10 倍,肥胖的 2 型糖尿病患者的 β 细胞凋亡频率增加了 3 倍。结论是,2 型糖尿病中 β 细胞质量减少,其潜在机制是 β 细胞凋亡增加。阻止细胞凋亡的治疗方法可能是 2 型糖尿病管理的重大新进展,这种方法实际上可能在一定程度上逆转疾病,而不仅仅是缓解血糖。
如何改善
总体原则:
1型糖尿病疗法:
T1D 是由于 β 细胞的自身免疫性破坏引起的,而 T2D 是由于 β 细胞质量和 β 细胞功能共同丧失而引起的,其中 β 细胞质量的丧失可能是由于 β 细胞功能障碍所致。寻找防止 β 细胞质量减少、保留剩余 β 细胞功能以及开发再生它们的方法,这是现在新的研究方向。成功抑制自身免疫和 β 细胞替代是开发成功的 T1D 疗法的关键组成部分。在过去的十年中,在利用干细胞、诱导多能干细胞 (iPS) 以及罕见的成体胰腺祖细胞、导管细胞和非胰腺细胞类型生成胰岛素生成细胞方面取得了重大进展。尽管干细胞和祖细胞在体外成功分化为胰岛素产生细胞,但该过程仍然效率低下,并且分化的细胞不成熟,胰岛素含量有限且缺乏葡萄糖刺激的胰岛素分泌(GSIS )。
2型糖尿病疗法:
2型糖尿病的特点是胰岛素分泌受损并伴有外周组织胰岛素抵抗。T2D 发展的主要原因是胰腺 β 细胞质量减少和 β 细胞功能受损。由于β细胞质量的减少仅与糖尿病的持续时间相关,有研究认为β细胞质量的减少不是糖尿病的原因,更可能是β细胞功能障碍的结果。有趣的是,减少胰岛素需求可以延缓疾病从胰岛素抵抗阶段进展为糖耐量受损(IGT)和糖尿病。用于保护β细胞功能的方法包括减轻体重和增加体力活动以提高胰岛素敏感性。噻唑烷二酮类 (TZD) 和二甲双胍等药物可以改善 IGT 患者的胰岛素抵抗,并防止其进展为 T2D。GLP-1 和 GLP-1 类似物代表另一类药物,它们通过改善 β 细胞功能和引发体重减轻来防止从 IGT 进展为 T2D。
1、生活方式改变
由于发现 T1D 和 T2D 是由于功能性 β 细胞量减少所致,因此增强 β 细胞量和功能的策略将有益于这两种类型的糖尿病。β细胞数量可以通过增强现有β细胞的增殖或通过在体内从非β细胞再生新的β细胞(即,通过新生/转分化)来增加。然而,应仔细评估此类疗法的后果,以增加不受控制的细胞生长的风险。除了增强 β 细胞增殖之外,糖尿病的另一种治疗策略是通过增强剩余 β 细胞群的功能来提高其有效性。
肥胖是T2DM的主要危险因素,肥胖患病率的增加是T2DM随之增加的主要原因。肥胖和缺乏体力活动会导致胰岛素抵抗并增加β细胞的工作量。减肥和运动干预可提高胰岛素敏感性并减轻 β 细胞的分泌需求。
美国糖尿病预防计划(DPP)表明,实施一项通过饮食和运动实现体重至少减轻7%的计划,可使糖耐量受损(IGT)患者的T2DM发病率降低58%。生活方式干预对降低 T2DM 发病率的作用与 β 细胞功能的整体改善有关,而β细胞功能的改善是由胰岛素敏感性的提高所驱动的,因此描述胰岛素分泌和胰岛素敏感性之间关系的双曲线向右移动。芬兰糖尿病预防研究 (DPS) 还显示,接受生活方式干预(包括减肥和增加体力活动)的 IGT 个体的 T2DM 发病率降低了 58% 。最近的一项 DPS 分析表明,生活方式干预有助于通过改善胰岛素敏感性来保护 β 细胞功能并预防 T2DM 的发展 。
2、药物及药物联合
GLP-1 受体激动剂:胰高血糖素样多肽-1 (GLP-1) 是一种肠促胰岛素激素,由肠道中的 L 细胞响应营养刺激而分泌。GLP-1 具有多种特性,使其成为治疗 T2DM 的理想药物。它可以增强葡萄糖刺激的胰岛素分泌,抑制胰高血糖素分泌,延迟胃排空并抑制食欲。但是GLP-1 被二肽基肽酶 4 (DPP-4) 裂解,导致其快速失活, 好在DPP-4 耐药的 GLP-1 受体激动剂,包括艾塞那肽和利拉鲁肽,以及 DPP-4 抑制剂已开发用于治疗T2DM 。β细胞质量的减少可以通过增强单个β细胞的功能来恢复。肠促胰岛素激素的使用代表了一种这样的疗法,它具有多种有助于改善糖尿病的生理益处。GLP-1 类似物和 DPP4 抑制剂可增强 β 细胞增殖、存活和分化。
最近一项针对肥胖成人的研究表明,与安慰剂相比,利拉鲁肽(剂量范围为每天 1.8 至 3 毫克)为期 20 周的治疗可带来更大的体重减轻,并且前驱糖尿病的患病率降低 84%–96%。另一项临床试验表明,在葡萄糖稳态受损(IGT 或 IFG)的肥胖参与者中,为期 24 周的艾塞那肽治疗加生活方式改变导致 77% 的体重减轻更大,糖耐量正常化,而安慰剂组的这一比例为 56% 。最近的一项随机对照试验表明,GLP-1 受体激动剂艾塞那肽可能对 T2DM 患者的血糖控制具有持久作用。
噻唑烷二酮类 (TZD):它是核转录因子过氧化物酶体增殖物激活受体-γ 的配体,具有广泛的作用。研究表明,TZD 可降低脂毒性,防止 β 细胞凋亡,增加血清脂联素水平,并改善 β 细胞功能 。预防试验一致表明,TZD 可有效预防高危患者 2 型糖尿病的发生约 50%–75%。ADOPT 研究表明,与二甲双胍和磺脲类药物相比,TZD 对最近诊断的 T2DM 患者的血糖控制具有显着更强的持久性,表明 TZD 可以通过改善胰岛素敏感性来保护 β 细胞功能并降低β细胞的分泌需求。
虽然胰岛素增敏可以降低胰岛素水平,提高胰岛素敏感性,但用药带来的副作用,如体重增加,是不可避免的,这会影响糖脂代谢受损患者的长期疗效。
二甲双胍:二主要通过抑制肝葡萄糖产生和增加胰岛素敏感性来有效降低高血糖。目前被推荐作为治疗T2DM的一线药物。体外研究表明,二甲双胍可以保护分离的人胰岛免受糖毒性和脂毒性,这表明二甲双胍可能对 β 细胞健康产生有益影响 。在临床研究中,DPP 表明二甲双胍可将 IGT 向 T2DM 的转化减少 31% ,表明它对减缓 T2DM 的进展具有适度的作用。
阿卡波糖:阿卡波糖是一种 α-葡萄糖苷酶抑制剂,通过抑制小肠酶的活性,导致葡萄糖吸收减少,从而改善餐后高血糖。预防 NIDDM (STOP-NIDDM) 的研究发现,与安慰剂相比,接受阿卡波糖治疗的血糖水平受损患者在 3.3 年内发生 T2DM 的相对风险降低了 25% 。然而,在停用阿卡波糖后的 3 个月观察期内,最初分配到阿卡波糖组的未转化患者的糖尿病发病率 (15%) 高于首先分配到安慰剂组,这表明停止积极治疗后,阿卡波糖的益处就会消失。
胰岛素:体外研究表明,缩短先前葡萄糖毒性的持续时间会增加恢复 β 细胞功能的可能性。因此,早期和更积极的治疗策略可以快速使新诊断的 T2DM 患者的血糖水平正常化,可以通过减少糖毒性来保留残余的 β 细胞功能。临床研究表明,早期短期(2-3 周)强化胰岛素治疗对新诊断的 T2DM 患者具有有益效果。
磺脲类药物:尚无临床研究证明磺脲类药物在预防 T2DM 方面具有有益作用。临床研究中观察到的磺酰脲类治疗缺乏持久性可能是由于其对胰腺 β 细胞具有潜在的破坏作用。对分离的人胰岛的研究表明,磺酰脲类、格列本脲可降低胰岛素含量,并诱导 β 细胞凋亡。
联合治疗:最近的一项临床研究检查了艾塞那肽和罗格列酮联合治疗与单独治疗相比对已服用二甲双胍的 T2DM 患者胰岛素敏感性和 β 细胞功能的影响。与单独治疗相比,艾塞那肽和罗格列酮的 20 周联合治疗可显着改善胰岛素敏感性和 β 细胞功能,并实现更好的血糖控制,表明联合治疗具有有益效果。
3、减肥手术
减肥手术是一种有效且持久的肥胖治疗方法,可显着改善肥胖 T2DM 患者的血糖控制。SOS 研究最近检查了减肥手术(LAGB、VBG、RYGB)对预防肥胖成人 T2DM 的影响,该研究对手术治疗和匹配对照进行了 15 年的跟踪。与标准治疗相比,减肥手术将肥胖成人患 T2DM 的长期相对风险降低了 78%,而在 IFG 患者中,减肥手术将 T2DM 的相对风险降低了 82%。术后死亡率为0.2%,2.8%的患者出现需要再次手术的并发症。这些研究结果表明,减肥手术对于肥胖成人(尤其是 IFG 患者)预防 T2DM 具有有效且持久的效果。
4、间歇性断食
间歇性禁食可以降低空腹血糖以及空腹胰岛素水平,隔日断食尤其明显,胰岛素水平的下降反映了胰岛素敏感性的增加。HOMA-IR是胰岛素抵抗指数,也是评价胰岛素敏感性的金标准。对 IF 饮食干预后胰岛素敏感性的分析表明,与典型口服胰岛素增敏吡格列酮的临床研究相比,胰岛素水平平均降低了 13.25 mU/L。
脂肪组织炎症是引起胰岛素抵抗的关键因素,脂肪细胞分化和脂肪细胞肥大导致炎症的恶性循环。因此,体重或内脏脂肪的减少意味着胰岛素敏感性的改善。间歇性断食大量研究表明,可以减轻体重,BMI平均下降0.8kg/m 2 (95% CI:−1.32; -0.28),体重平均下降1.87 kg ,腰围平均减少 2.08 厘米。
仅靠饮食干预就达到了改善胰岛素敏感性的理想效果。这种改善生活方式的辅助疗法值得推荐。尽管3个月内血糖和HbA1c尚未显着改善,但随着胰岛素敏感性的显着改善,长期的血糖控制改善是可期的。
5、饮酒
通常急性酒精会抑制肝脏糖原的分解,饮酒后,胰岛素的敏感性会提高,身体开始以更快的速度处理糖,这导致糖代谢激增,低于正常水平。根据美国的研究,在现实环境中,饮用酒精饮料可使餐后血糖降低 16-37%,饮酒之后夜间血清生长激素、皮质醇和胰高血糖素反应降低,造成隔日清晨低血糖。是不是乍听上去喝酒可以改善胰岛素抵抗,日本2020年一项研究发现,长期适度饮酒者30–60 克/天,与日本男性的胰岛素抵抗和脂肪肝呈负相关。
总结
T2DM 发病率的迅速上升与肥胖率的类似上升相呼应,肥胖率会导致胰岛素抵抗,并可能对 β 细胞健康产生额外影响。减少体内脂肪(例如饮食和运动、GLP-1 受体激动剂或减肥手术)或改变脂肪生物学 (TZD) 的干预措施为减缓或阻止导致 T2DM 的 β 细胞功能恶化提供了最佳证据。
[1] Prevalence and Treatment of Diabetes in China, 2013-2018. JAMA. 2021 Dec 28;326(24):2498-2506. DOI: 10.1001/jama.2021.22208.
[2] Morbidity and mortality after lifestyle intervention for people with impaired glucose tolerance: 30-year results of the Da Qing Diabetes Prevention Outcome Study. Lancet Diabetes Endocrinol. 2019 Jun;7(6):452-461. DOI: 10.1016/S2213-8587(19)30093-2.
[3] Kathleen A. Page and Tamar Reisman,Interventions to Preserve Beta-Cell Function in the Management and Prevention of Type 2 Diabetes,Curr Diab Rep. Author manuscript; available in PMC 2014 Apr 1.
and Tamar Reisman,Interventions to Preserve Beta-Cell Function in the Management and Prevention of Type 2 Diabetes,Curr Diab Rep. Author manuscript; available in PMC 2014 Apr 1.













还没有评论,来说两句吧...